
Abbiamo visto in articoli precedenti che le comuni nozioni di Calore e Temperatura non sono proprietà intrinseche della materia ma sono la nostra percezione del perenne moto vibrazionale (agitazione termica) degli atomi di cui la materia è fatta.
Il trasferimento di calore da un corpo all’altro è in realtà un trasferimento di agitazione termica dall’uno all’altro che si traduce in un abbassamento della temperatura del corpo che cede agitazione termica e di un innalzamento della temperatura del corpo che la riceve. Fortunatamente madre natura ha progettato noi umani in modo tale da avere quella particolare percezione che ben conosciamo, specialmente quando avviciniamo una mano al fuoco!
Vogliamo ora mostrare con un semplice esperimento in cucina che anche la comune nozione di Pressione di un gas (o vapore) è determinata dalla agitazione termica degli atomi.
Vediamo cosa succede quando la mattina riscaldiamo il latte. Prima di procedere, facciamo un tuffo nell’infinitamente piccolo del latte.
Il latte è composto per circa l’85% di acqua, il restante 15% è composto da residuo secco, proteine e grassi.

L’acqua è fatta di molecole molto semplici, un atomo di Ossigeno (O) legato a due atomi di Idrogeno (H). In una goccia d’acqua le molecole sono tenute insieme da forze molecolari tali per cui la goccia può cambiare forma, scorrere ma non svanire. Al crescere della temperatura cresce l’agitazione termica degli atomi e quindi delle molecole finché a un certo punto la forza di attrazione tra le molecole non è più sufficiente a tenerle insieme, le molecole si staccano e volano via: abbiamo descritto la formazione del vapore d’acqua. Osserviamo che alla superfice di separazione acqua-aria c’è vapore acqueo a qualsiasi temperatura tra 0 °C e 100 °C, ovviamente in quantità crescenti al crescere della temperatura dell’acqua.
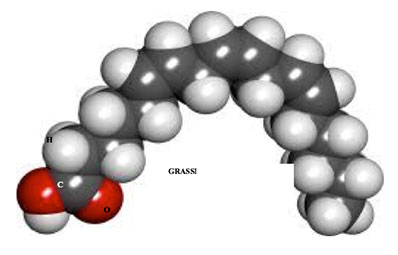
I grassi hanno struttura atomica più complessa. Essi sono costituiti da lunghe catene di atomi di Ossigeno, Idrogeno e Carbonio (C), tenute insieme da forze ben superiori a quelle tra molecole d’acqua cosicché al crescere della temperatura tali catene, pur aumentando la loro agitazione termica, tendono a conservare la loro struttura fino a temperature oltre i 100 °C (per esempio, la temperatura di fumo dell’olio d’oliva, alla quale i grassi cominciano ad alterarsi, è intorno ai 200 °C).

Mettiamo ora la nostra pentola con il latte sul fuoco. Man mano che il latte si scalda si forma una sottile pellicola sulla sua superficie. Ciò è dovuto al fatto che i grassi del latte si separano dalla massa liquida e vengono in superficie dove, in virtù della loro intricata struttura, tendono a incollarsi insieme formando la pellicola.
Contemporaneamente, l’acqua contenuta nel latte riscaldandosi genera bolle di vapore d’acqua che salgono verso la superficie ma non possono disperdersi nell’aria perché sono bloccate dalla pellicola. Al crescere della temperatura la loro quantità e agitazione termica aumenta per cui i loro urti con la pellicola diventano sempre più frequenti e più intensi traducendosi in una pressione crescente sotto la pellicola di modo che essa si gonfia e tende a salire.

Il processo accelera violentemente quando il latte arriva alla temperatura di circa 90°C, fino a far traboccare dalla pentola. Sappiamo che rimescolando il latte si evita il trabocco, e ciò perché così facendo si lacera la pellicola superficiale liberando la pressione delle bollicine di vapore d’acqua. In conclusione, come per il Calore e la Temperatura, anche la nozione di Pressione di un gas è riconducibile all’agitazione termica degli atomi della materia.
Ora modifichiamo leggermente il nostro apparato sperimentale. Sostituiamo il latte con acqua, magari mettiamoci del riso da cuocere, chiudiamo la pentola con un coperchio a tenuta ermetica e…
voilà abbiamo fatto una pentola a pressione!
La temperatura di ebollizione dell’acqua è 100 °C alla pressione atmosferica al livello del mare, cioè 1 Atmosfera. Se la pressione dell’aria è inferiore (come in alta montagna) la temperatura di ebollizione è più bassa di 100°C, mentre se la pressione è più alta anche la temperatura di ebollizione si alza oltre i 100 °C. In una qualsiasi pentola tradizionale, usata nelle usuali condizioni ambientali, l’ebollizione dell’acqua avviene quindi ad una temperatura intorno ai 100 °C, indipendentemente dall’intensità del calore sviluppato dai fornelli. Infatti, al momento di bollire, l’acqua evapora e sottrae calore al liquido ed alla pentola. Fin tanto che ci sarà liquido in grado di evaporare e fuoriuscire, nessun calore aggiuntivo potrà innalzare la temperatura al di sopra dei 100°C in condizioni di pressione atmosferica normale.

Con la pentola a pressione è invece possibile bloccare la fuoriuscita di aria e vapore, in tal modo al suo interno la pressione aumenterà fino a 2 Atmosfere (sarà dunque doppia rispetto a quella riscontrabile nell’ambiente esterno). Il punto di ebollizione dell’acqua, quindi, sarà innalzato a valori di 120 °C o superiori, permettendo alle pietanze di cuocere in tempi ridotti. Per evitare pressioni e temperature troppo alte, la cottura è regolata da due valvole, una di controllo e una vera e propria valvola di sicurezza. È questa la principale innovazione tecnica sulla quale si basa la cottura a pressione: al raggiungimento della pressione prevista, la forza esercitata dal vapore sulla valvola di controllo eguaglierà quella esercitata dal suo peso, sollevandola e facendo uscire vapore acqueo, regolando così la pressione interna al valore desiderato (circa 2 Atmosfere). Se la valvola di controllo per qualche motivo si blocca allora interverrà la valvola di sicurezza evitando spiacevoli incidenti.

Luigi Catalani nasce a Norma (LT) nel 1946. Si laurea in Ingegneria Elettronica con indirizzo Calcolatori e Controlli Automatici nel 1975. E’ assunto da una società romana leader nel settore della Meccanottica di precisione occupandosi di progettazione elettronica e software di sistemi di Aereofotogrammetria per applicazioni cartografiche civili e militari. Nel 1980 è assunto da una primaria azienda Aerospaziale italiana come dirigente del reparto progettazione e sviluppo di apparati avionici di bordo per aerei ed elicotteri militari e civili. Nel 1988 passa alle dipendenze di una società romana leader nel settore dei sistemi di difesa avionica con l’incarico di Project Manager per diversi contratti internazionali per lo sviluppo e produzione di apparati destinati alle aeronautiche di Italia, Germania, UK e Spagna. Nel 2007,nella stessa società, conclude la sua carriera in qualità di Responsabile Commerciale degli stessi contratti.


