
E’ domenica mattina, c’è un bel sole e Lucrezia decide di andare a fare un po’ di jogging nel parco vicino casa. Indossa la sua bella tuta e le sue scarpe da ginnastica appena comperate: sono bellissime, bianche con delle strisce blu e la suola è di gomma molto flessibile e morbida.
Cos’è la “gomma”?
La gomma arrivò in Europa in seguito alla scoperta dell’America.
Si chiamava caucciù che significa “legno che piange”: un liquido denso e appiccicoso ricavato dalla pianta HEVEA BRASILIENSIS (famiglia delle Euforbiacee).

Nel 1770 il grande chimico inglese Priestley scoprì che il caucciù indurito cancellava i segni di matita e così inventò la gomma da cancellare.
Il caucciù a temperature relativamente basse induriva diventando rigido e fragile mentre al caldo rammolliva fino a diventare filante e appiccicoso.
Nel 1783 si scoprì che questa gomma risultava solubile in TREMENTINA (una resina vegetale oleosa, chiara, fluida e volatile).
Con questa soluzione i fratelli Montgolfier impregnarono il tessuto dei loro palloni aerostatici (impermeabile quindi all’acqua e ai gas).

Nel 1803 nacque a Parigi la prima fabbrica di gomma, ma non era ancora stato risolto il problema della temperatura.
Nel 1839 il chimico americano Charles Goodyear inventò la “vulcanizzazione” della gomma che consisteva nell’aggiungere, durante la lavorazione della stessa, dello ZOLFO.
Questo processo migliorava le caratteristiche meccaniche e di resistenza nei confronti di variazioni di temperatura, abrasioni, agenti chimici etc.
Nel 1895 i fratelli Michelin introdussero l’uso della gomma vulcanizzata nella produzione di gomme per le ruote delle automobili (ancora oggi le gomme delle nostre auto sono fatte con questo processo).

A fine ‘800 primi ‘900 i chimici faticosamente capirono che il costituente principale della gomma era un composto chiamato ISOPRENE, per la precisione un POLIMERO dell’ISOPRENE (tante molecole di questo prodotto attaccate l’una all’altra).
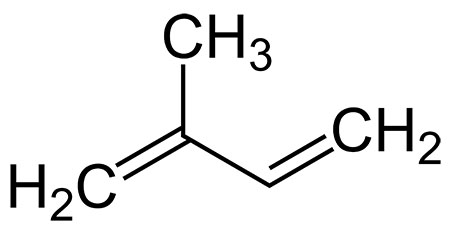
I polimeri che presentano un elevato grado di elasticità, capaci cioè di riprendere la propria forma originaria, dopo aver subito deformazioni, sono chiamati ELASTOMERI.
Al giorno d’oggi la stragrande maggioranza delle scarpe che utilizziamo sono fatte di ELASTOMERI.
Pensate: ogni volta che indossiamo questa tipologia di scarpe indossiamo “CHIMICA”.
Gli attuali ELASTOMERI non derivano più dal caucciù ma dagli idrocarburi estratti dal petrolio.

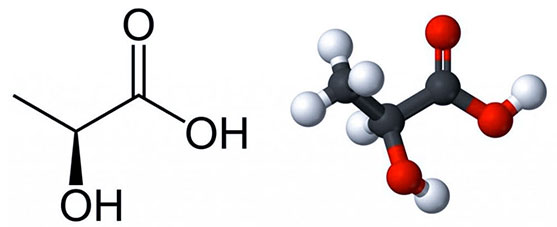
Lucrezia, dopo una lunga sgambata, torna casa e si sdraia sul divano con un fastidioso dolore ai muscoli delle gambe: evidentemente è l’ACIDO LATTICO che si è accumulato nel suo tessuto muscolare.

I nostri muscoli, per poter funzionare, necessitano di energia. Nel nostro organismo l’energia viene principalmente fornita dalla degradazione della nostra riserva di ZUCCHERI. In questo processo gli ZUCCHERI vengono degradati dall’OSSIGENO fino ad arrivare ad acqua e anidride carbonica.
Se l’attività muscolare è molto intensa, e anche se non si è molto allenati (è il caso di Lucrezia), la quantità di ossigeno presente nei tessuti non è sufficiente a completare la degradazione degli zuccheri che si ferma ad ACIDO LATTICO che si accumula nelle cellule e quindi nei muscoli dando dolore.
L’ACIDO LATTICO è un prodotto che non può essere utilizzato dalla cellula per produrre energia, di conseguenza viene trasportato nel fegato dove viene convertito in glucosio, questo zucchero viene di nuovo trasferito nei muscoli dove viene degradato per produrre energia.
L’accumulo di ACIDO LATTICO e, di conseguenza, dolore non è altro che un campanello d’allarme che il nostro corpo ci invia per avvisarci che siamo in una situazione di EMERGENZA!
Quanto detto non è estremamente AFFASCINANTE?
LA CHIMICA IN VERSI
di Alberto Cavaliere
BORO
S’ottiene libero dal sal borace,
seguendo un metodo molto efficace:
si parte, in genere, da quel prodotto
borato sodico – che vien ridotto
con il magnesio polverizzato;
con il cloridrico dopo è trattato
e con l’idracido, indi, del fluoro:
amorfo, in polvere bruna, s’ha il boro.
Nell’alluminio fuso si scioglie,
e raffreddandolo, poi, si raccoglie
in chiari, splendidi, duri cristalli.
Dei metalloidi. non dei metalli,
esso ha i caratteri suoi principali:
quindi dà gli acidi, dà quindi i sali.
E tra i molteplici sali formati
sono i notevoli tetraborati,
onde utilissimo riesce il boro,
anzi l’analisi ne fa un tesoro.
In quanto agli acidi, ve ne son tre:
v’è l’ortoborico, noto perché
esiste libero da noi in Toscana
e dai boriferi “soffioni ” emana.
Fra i più pregevoli medicinali,
bianco insolubile, dà molti sali.
Il metaborico non è costante;
bianco insolubile, poco importante.
E tetraborico l’ultimo è detto:
vetroso fragile bianco d’aspetto.
sette d’ossigeno, quattro di boro
e due d’idrogeno, messi tra loro,
ne dan la formula, allineati.
i sali chiamasi tetraborati.
Di quello sodico poi non si tace,
perch’è notissimo, perch’è il borace.
Sappiam che libero questo non manca,
ed è una polvere leggera e bianca.
S’usa in analisi per i metalli:
quando si scaldino i suoi cristalli
fino a un altissimo grado, di norma,
si disidratano: ei cambia forma;
se ancor riscaldasi, fonde ed allora
discioglie gli ossidi e li colora.

Fausto Bonifacio nasce a Milano nel 1951, si laurea in Chimica Pura nel 1975 e dopo un anno di servizio militare viene assunto, presso un’importante azienda farmaceutica milanese, con la mansione di operatore di laboratorio di ricerca.
Nel 1988 emigra, al contrario, nella città di Frosinone e prende servizio quale direttore della funzione Ricerca e Sviluppo di una nota azienda chimico-farmaceutica operante nel settore della sintesi e produzione di principi attivi .
Nel 1998 viene assunto, con la qualifica di direttore Ricerca e Sviluppo, da una nota azienda chimico-farmaceutica situata nei pressi di Latina e ricopre inoltre lo stesso incarico nella consociata spagnola di tale azienda.
Nel 2004 emigra in toscana presso un’importante azienda chimico-farmaceutica dove ricopre la carica di direttore di stabilimento fino al 2013 quando cessa l’attività lavorativa godendosi poi la meritata pensione.
Attualmente vive e saltuariamente lavora a Latina.



Un commento su “La Chimica intorno a noi – #18- La gomma e l’Acido Lattico”